Dopo oltre 50 anni, una nuova classe di antibiotici contro un ceppo di batteri multi-resistente Acinetobacter baumannii raggiunge la prima fase di trial clinico. Questo risultato deriva dallo sforzo congiunto di ricerca accademica e delle aziende farmaceutiche di Stati Uniti ed Europa.
Il trattamento di infezioni batteriche è alla base della medicina moderna, le cui fondamenta sono ora messe in discussione dall’aumento di patogeni antibiotico-resistenti. È quindi urgente lo sviluppo di nuovi strumenti contro questa minaccia globale per la salute pubblica.
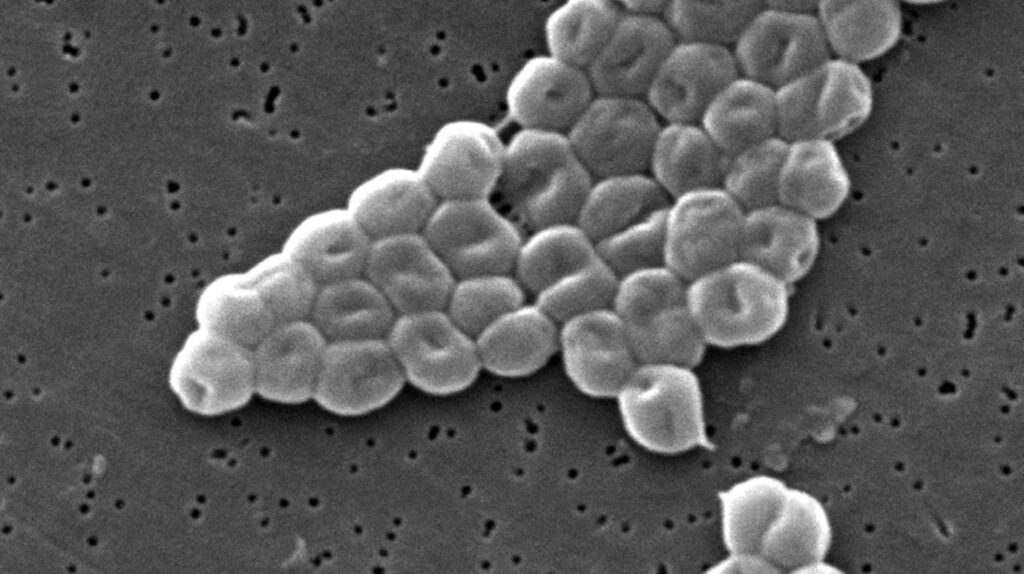
Acinetobacter baumannii è in cima alla lista degli agenti patogeni prioritari per la ricerca e sviluppo di nuovi antibiotici, elaborata dall’Organizzazione mondiale della sanità (Oms) nel 2017. Questo microrganismo, fa parte di un gruppo di patogeni ribattezzati “ESKAPE”: Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa e diverse specie di Enterobacter. Questi sono i batteri più comunemente presenti in ospedali e luoghi di assistenza sanitaria, che hanno sviluppato strategie per evadere i trattamenti con i farmaci attualmente in uso, e sono quindi un obiettivo primario d’interesse sanitario.
Negli ultimi anni, la ricerca scientifica ha accelerato nel campo dell’ antibiotic discovery sfruttando tutti gli strumenti a sua disposizione, inclusi nuovi sistemi di deep learning che hanno dimostrato risultati incoraggianti per ottimizzare la ricerca e sviluppo di nuovi antibiotici contro i patogeni ESKAPE.
Nuova classe di antibiotici ora in clinical trial
Due studi pubblicati sulla rivista scientifica Nature a inizio gennaio propongono una nuova classe di antibiotici contro le infezioni da A. baumannii. Uno dei composti identificati (zosurabalpin) è già in clinical trial. Anche se la strada per un’eventuale approvazione rimane ancora lunga, questo è da considerarsi già un notevole risultato: per quanto riguarda gli antibiotici con nuovi meccanismi d’azione, solo uno su trenta candidati solitamente supera la fase pre-clinica.
Questi studi hanno visto la partecipazione di ricerca accademica e aziende farmaceutiche di varie parti del mondo: i ricercatori di Harvard e del Sanford Burnham Prebys Medical Discovery Institute di San Diego hanno unito le forze con le aziende farmaceutiche Roche in Svizzera, Janssen Research & Development in Belgio e Aptuit (Evotec) a Verona. La fase clinica ora avviata sarà importante per valutare l’eventuale sviluppo di resistenze nei pazienti.
Colpire la barriera esterna per indebolire il patogeno
A. baumannii è un tipo di batterio particolarmente resistente, che può sopravvivere per settimane sulle superfici grazie alla sua doppia membrana cellulare, una sorta di doppia pellicola protettiva, la quale blocca anche l’ingresso di molti antibiotici. Inoltre, la flessibilità del suo metabolismo e la sua capacità di scambiare materiale genetico con altri batteri hanno fatto sì che questo patogeno diventasse, in molti casi, resistente anche ai pochi antibiotici in grado di penetrare la sua membrana.
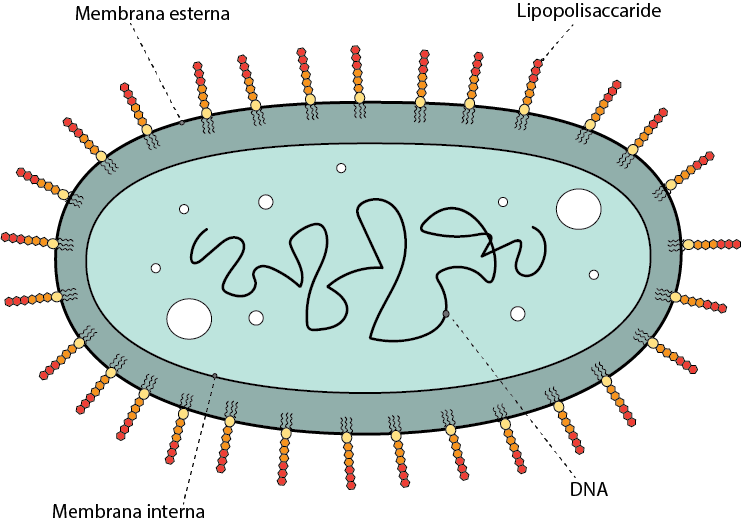
I lipopolisaccaridi (LPS), molecole composte da grassi e zuccheri, sono uno dei componenti principali della membrana esterna di questi batteri. Per l’assemblaggio della membrana esterna i LPS vengono trasportati dalla membrana interna a quella esterna; la nuova classe di farmaci mira a bloccare questo passaggio, per compromette l’integrità della membrana esterna e aumentare la suscettibilità del batterio agli antibiotici.
Altri farmaci utilizzati in precedenza puntavano a distruggere questo sistema, ma A. baumannii era riuscito ad aggirarli: la nuova classe sfrutta un nuovo bersaglio all’interno di questo passaggio di assemblaggio. Tramite studi strutturali, biochimici e genetici, i ricercatori hanno individuato dei composti – chiamati small molecule (piccole molecole) – che funzionano da “trappola”, legando contemporaneamente il fattore responsabile del trasporto tra le membrane e la molecola di LPS. Questa classe di farmaci si è dimostrata efficace nell’ eliminazione del patogeno sia in provetta che in modelli pre-clinici.
La ricerca riparte, ma l’economia deve supportarla
Come già riportato su Agenda17, gli ostacoli allo sviluppo di nuovi antibiotici non sono solo scientifici: mancano supporto finanziario e gli incentivi economici per le aziende.
Lo sviluppo di un nuovo antibiotico ha costi stimati che possono raggiungere 1 miliardo di dollari per l’azienda, ma una volta in commercio le previsioni di profitto sono meno di 100 milioni l’anno, visto l’uso sporadico di questi farmaci. Gli esperti invitano infatti a un utilizzo moderato di antibiotici per evitare lo sviluppo di ulteriori resistenze ai farmaci.
Arrivano dai Paesi anglosassoni strategie per nuovi approcci economici: lo scorso aprile è stato riproposto negli Stati Uniti il Pioneering Antimicrobial Subscriptions to End Upsurging Resistance (PASTEUR) Act, che propone un modello di finanziamenti “basato su abbonamento”, simile a quello lanciato recentemente dal Regno Unito. Secondo questo approccio, lo Stato dovrebbe pagare in anticipo l’accesso agli antibiotici, indipendentemente dal numero di farmaci venduti, in modo che i finanziamenti non siano limitati e limitanti per la ricerca e lo sviluppo di nuovi farmaci.
In occasione della pubblicazione dei nuovi risultati, la rivista scientifica Nature pubblica nel suo editoriale del 4 gennaio a una Call to action ai governi per supportare lo sviluppo di nuovi antibiotici con piani di finanziamenti a lungo termine. La ricerca sta facendo la sua parte, ma non può agire da sola: “Senza un piano di finanziamenti strategico, questi nuovi farmaci potrebbero rimanere sullo scaffale per anni”.

